患者故事 | 鲁道夫的“药柜”——打开一部慢乙肝治疗药物的发展史
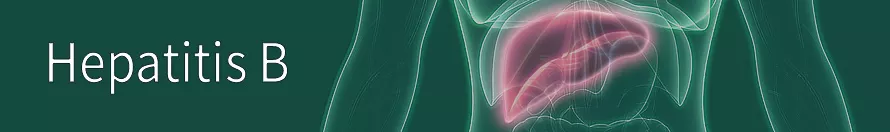 (图片来源:CDC)
(图片来源:CDC)
傍晚时分,鲁道夫习惯性地打开了桌子上印着Viread®(富马酸替诺福韦酯)的药瓶,倒出一粒,服了下去。有些吃完了的药瓶被鲁道夫小心地存放在一个大大的储物间里,那里同样摆着很多空瓶。鲁道夫用这种方式在记录着这些年自己同病魔斗争的日子[1]。
鲁道夫经常在网站上分享自己的经历。鲁道夫说自己永远忘不了那一天,他一脸震惊地看着体检报告,怎么都不肯相信自己身强力壮,竟然会患上乙型肝炎。
可现实就是这样,永远不会按套路出牌。
 (图片来源:pixabay.com)
(图片来源:pixabay.com)
十几年前,自己患病的消息对于鲁道夫来说犹如晴天霹雳,那个发誓要在华尔街叱咤风云的男子开始一蹶不振。好在,在家人和朋友的鼓励下,鲁道夫决定积极接受治疗。当时得益于一种叫富马酸替诺福韦酯(TDF)的口服抗病毒药物,鲁道夫受损的肝组织已经恢复大半,血清HBV-DNA也已经变为阴性。
富马酸丙酚替诺福韦(TAF),更是在2016年得到美国FDA批准用于12岁以上青少年和成年人的乙型肝炎治疗药物[2]。如今,TAF已经帮助了全球数以万计的乙型肝炎患者。可在这之前,鲁道夫和很多慢性乙型肝炎患者一样,都经历了一段很长时间的换药过程。
尤其在回顾鲁道夫换药历程的时候,我们发现,鲁道夫的换药史简直就是一部活脱脱的乙型肝炎治疗药物发展史。
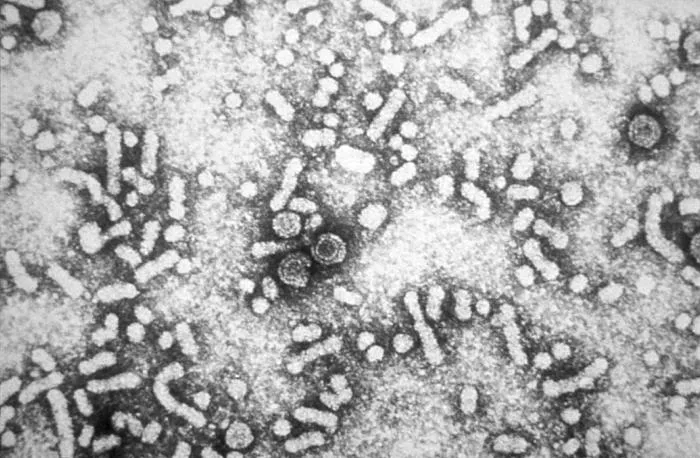
 自从1963年巴鲁克.布隆伯格(Baruch S. Blumberg)和他的同事们在澳大利亚土著人血清中发现了“澳抗”,即乙肝表面抗原后,乙肝的神秘面纱开始被揭开。7年后,乙肝病毒的结构被人类完全破解,直径为42nm的Dane颗粒展现在人类的面前[3]。
自从1963年巴鲁克.布隆伯格(Baruch S. Blumberg)和他的同事们在澳大利亚土著人血清中发现了“澳抗”,即乙肝表面抗原后,乙肝的神秘面纱开始被揭开。7年后,乙肝病毒的结构被人类完全破解,直径为42nm的Dane颗粒展现在人类的面前[3]。
 (图片来源:wiki)
(图片来源:wiki)
乙型肝炎病毒的发现,尤其是有研究证实了乙型肝炎病毒与肝癌发生风险增加63%有关以后,人们开始意识到感染乙型肝炎带来的严重后果[4]。
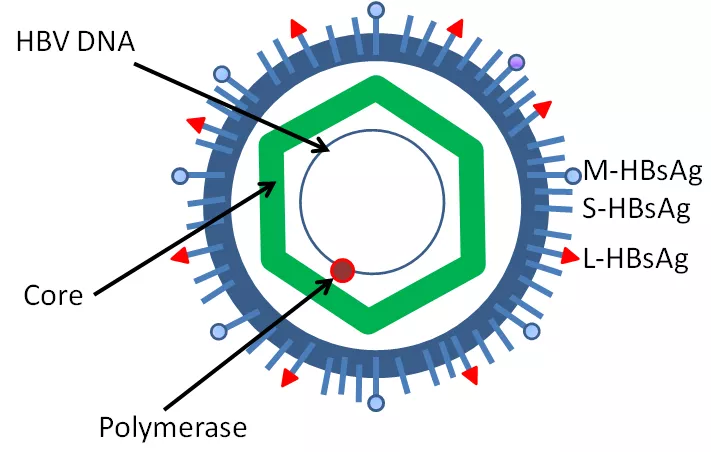
我们知道,乙型肝炎病毒在进入肝细胞以后,在DNA聚合酶的作用下,会形成一个共价闭合的环状DNA(cccDNA),cccDNA是乙型肝炎病毒前基因组RNA复制的原始模板,虽然其含量较少,每个肝细胞内只有约5~50个拷贝,但对乙型肝炎病毒的复制以及感染状态十分重要。
更重要的是,cccDNA半衰期特别长,很难从体内清除,这也是乙型肝炎病毒难以从体内清除的原因。
(图片来源:wiki)
这些原因在很大程度上增加了抗乙型肝炎病毒药物研发的难度,让治疗乙型肝炎成为了一个非常棘手的问题。
第一种用来治疗乙型肝炎的药物是干扰素——IFNα。干扰素是一种免疫调节剂,它可以提高我们自身的免疫调节能力,增加NK细胞的杀伤力。说白了就是干扰素会增加我们抵御病毒的能力[5]。
然而实际上,患者注射干扰素以后能否提高免疫力还要因人而异,而且以皮下注射的方式会导致患者依从性降低,最重要的就是干扰素会给患者带来一些副作用,比如流感样症状、骨髓抑制等。这也成为了欧美接受干扰素治疗的患者比例不超过10%的主要原因[6]。
 (图片来源:pixabay.com)
(图片来源:pixabay.com)
当时很多乙型肝炎患者都觉得注射干扰素太痛苦了,盼望着能有一种可以口服的抗病毒药物出现。
不得不说,鲁道夫是幸运的,就在上个世纪末,历史上第一款口服治疗乙型肝炎的抗病毒药物拉米夫定(Lamivudine,LAM)问世了[7]。1998年,拉米夫定的出现改变了很多乙型肝炎患者的命运。
拉米夫定是一种核苷类似物,核苷类似物在药学上也被称为竞争性抑制剂,它可以有效抑制有逆转录活性的乙型肝炎病毒DNA聚合酶,干扰乙型肝炎病毒DNA的合成,从而实现阻止乙型肝炎病毒复制的目的。
因此,在医生的建议下,鲁道夫尝试了拉米夫定。根据当时的临床研究结果显示,拉米夫定不仅降低了肝硬化、肝癌的风险,而且治疗一年可使HBeAg阴性患者血清HBV DNA下降60%-70%[8]。
事实确实如此,在服用拉米夫定一年以后,鲁道夫的各项指标都有所好转。
可谁想好景不长,很快鲁道夫的病情加重了。
是的,拉米夫定耐药了。随着服药时间的增加,越来越多的患者开始出现不同程度的耐药,有研究人员在对拉米夫定治疗情况进行回顾时发现,随着治疗时间延长,拉米夫定的耐药率也在增加,治疗第一年、两年、三年和四年耐药的发生率分别为14%、38%、49%和66%[9]。
耐药导致病情的反复也让很多像鲁道夫一样的患者苦不堪言,明明治疗得不错,一出现耐药所有的努力就又付之东流了。因此,研发新药解决拉米夫定耐药,成为了当时众多科研人员要解决的首要问题。
在这样的环境下,一些新的核苷(酸)类似物相继问世,包括2002年获批的阿德福韦酯(Adefovir,ADV)、2005年获批的恩替卡韦(Entecavir,ETV)、以及2006年获批的替比夫定(Telbivudine,LdT)[10]。
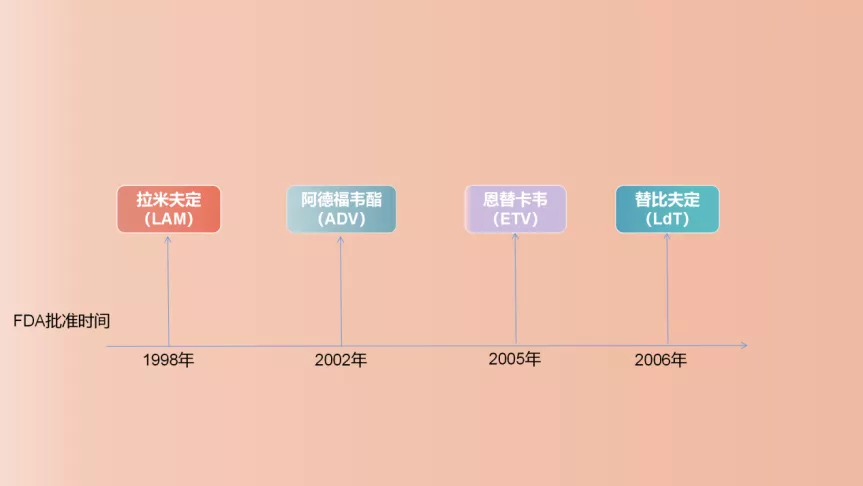
这三种药物都有不错的抗病毒效果,不过也都有各自的优缺点。
阿德福韦酯(ADV),是第一个治疗乙型肝炎的核苷酸类似物,虽然一问世就成为了拉米夫定耐药患者的有效替代药物,不过在带来效果的同时,也会给患者带来一定程度的肾脏和骨骼负担[11]。
恩替卡韦(ETV)是一种核苷类似物,在治疗2周内实现快速病毒抑制方面优于拉米夫定[12],且耐药屏障度相对较高,对未接受过抗病毒药物治疗的患者来说,是个不错的选择。但是有研究显示,对拉米夫定耐药的患者再服用ETV治疗,五年的耐药率将升至51%[13]。
替比夫定(LdT)也是一种核苷类似物,服用后不仅存在耐药问题,部分患者还可能会出现肌酸激酶增高,横纹肌溶解以及乳酸酸中毒等现象[14]。
 (图片来源:pixabay.com)
(图片来源:pixabay.com)
以上这些核苷(酸)类似物的出现看似给乙型肝炎病毒带来了沉痛的打击,但是药物的副作用以及耐药问题并没有得到彻底的解决。同时这些药物的缺陷也代表着患者们的诉求,需要有更简单有效、更安全的抗病毒药物,事实上,药物的研发也正在进行中。

在抗病毒药物的研发上,吉利德一直走在前面。
1997年,吉利德科学研究团队发现替诺福韦(tenofovir disoproxil,TFV)有抗HIV的能力以后,TFV这个化合物开始走进人们的视野[15]。
虽说最初合成的TFV存在抗病毒的潜力,但是TFV渗透性很差,口服时无法透过肠壁,药物利用率很低。
为了发挥TFV真正的药效,吉利德科学的研究团队经过反复的测试,在TFV结构的基础上,加上一个磷酸基团,研发出了富马酸替诺福韦酯(tenofovir disoproxil fumarate,简称TDF)。
TDF是TFV的前体药物,加上了磷酸基团的TFV口服后可以被肠道迅速吸收。2001年,TDF更是获得美国FDA批准成为了用于治疗艾滋病的药物。鉴于TDF良好的抗病毒效果,吉利德研究团队认为,TDF或许也可以用来治疗乙型肝炎。
于是,关于TDF治疗HBV感染的临床试验陆续展开,根据两项随机双盲对照研究48周结果显示,与ADV相比,TDF不仅显现了更高的乙型肝炎病毒清除率,而且临床随访8年尚未有临床耐药病案的报告[13]。
TDF早在做临床试验的时候,很多HBV感染者就对它充满期待,鲁道夫也是如此。在经过医生同意后,抱着试试看的心态,鲁道夫服用了TDF,没想到效果意外的好,服用不久之后,鲁道夫的血清HBV DNA便开始下降。
终于在2008年,TDF获得FDA批准,成为了继阿德福韦酯(ADV)之后获批的第二个核苷酸类似物。此外,因为TDF不错的疗效和优势又加之没有耐药发生,自从获批之后,它相继被WHO、美国、欧洲等国际指南推荐为一线治疗药物。
各种抗病毒药物的耐药情况
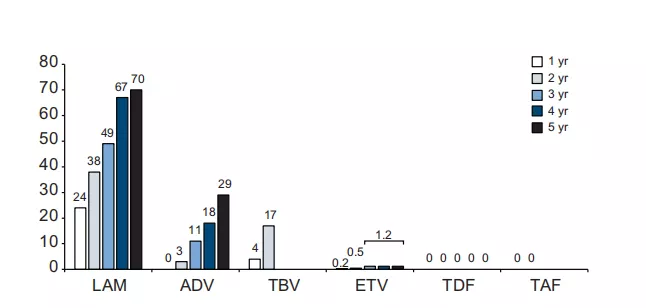 (图片来源:参考文献[17])
(图片来源:参考文献[17])
那么TDF就这么完美吗?一点缺点都没有吗?
其实也不是,TDF在肾脏毒性和骨骼影响等方面的确存在缺陷。
中国有句不成文的古话,叫“是药三分毒”。虽说不见得一定对,但是也不是全无道理的。随着乙型肝炎患者年龄增大,各种合并症和合并用药的比例增高;而长期服用TDF可能会存在肾功能不全、低磷性骨病的风险[18]。
因此,怎么提高药物利用率,避免肾脏毒性的同时,又能高效抑制病毒复制是当时乙型肝炎药物研发必须破解的难题。
上文也提到,TDF之所以可以被肠道吸收,是因为它在TFV结构的基础上加了一个磷酸基团。
看到这有人可能会说,不就是多一个基团吗?有这么神吗?
大家可不要小看这些磷酸基团的设计,一个好的磷酸基团可以显著提高药效,减少副作用,往往决定了一款药物的成败。
因此,当时吉利德科学的研究团队一致认为,想要提高药代动力学,减少副作用,还得重新设计一个基团,给TDF升升级才行。
 (图片来源:pixabay.com)
(图片来源:pixabay.com)
那么到底怎么设计新的磷酸基团呢?当时的研究人员首先想到了ProTide技术,ProTide技术是一种最具有结构多样性的前药策略。该技术的核心就是用一个芳香取代基模体和一个氨基酸酯组成的结构以磷酰胺酯的形式作用于细胞。加上了磷酰胺酯的药物就可以更加高效地进入细胞内[19]。
于是搭载了磷酰胺酯的TFV,犹如涅槃重生,新的前体药物富马酸丙酚替诺福韦(tenofovir alafenamide Fumarate,简称TAF)问世了。
变身之后的TAF,尽管有效成分依旧是替诺福韦(TFV),但是在药代动力学上有了明显的提升,只需要不到TDF十分之一的剂量就可以达到同等的抗病毒效果,还大大减少了副作用[20]。
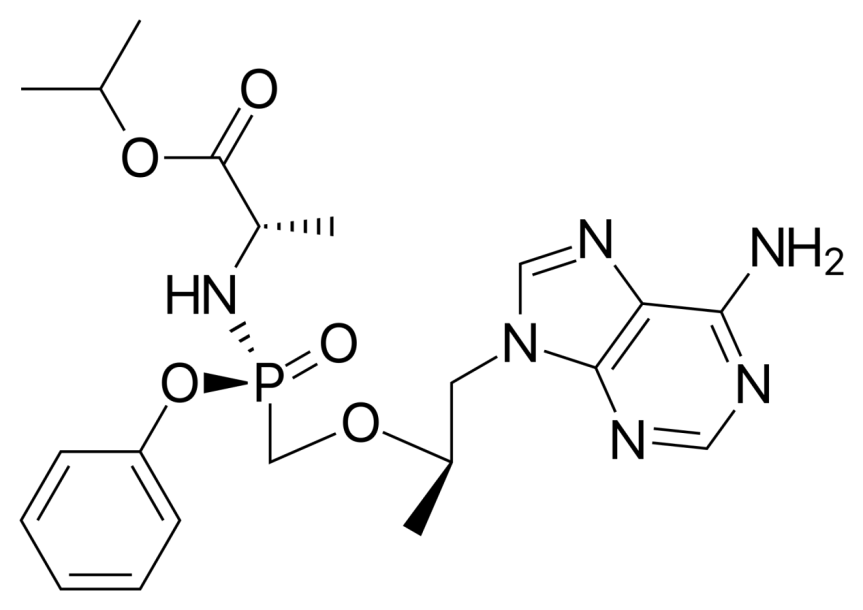 (图片来源:wiki)
(图片来源:wiki)
所以说,真的不要小看一个磷酸基团的作用,这个小小的磷酰胺酯不仅创造了丙肝治疗药物索磷布韦(Sofosbuvir)的传奇,还实现了TFV的新生,现在更是有“人民的希望”之称的瑞德西韦(Remdesivir)的结构特点。
至于TAF治疗乙型肝炎的效果如何,那就需要临床研究的数据来证明了。
在有关TAF的两项国际Ⅲ期临床研究中,研究人员将TAF与TDF的使用效果进行了对比。
研究共涉及1299名初治和经治的成年HBeAg阴性和HBeAg阳性的慢性乙型肝炎患者。其中108试验针对的是426名HBeAg阴性患者,110试验针对的是873名HBeAg阳性患者,研究人员将患者随机分配(2:1),根据血浆HBV DNA浓度和以前的治疗状态进行分层,分别给予每日一次口服TAF(25mg)或TDF(300mg),按剂量与安慰剂相匹配[20,21]。
两项研究的主要终点是在第48周时,血浆HBV DNA水平低于29 IU / mL的乙型肝炎患者比例。次要终点是在第48周时,髋部与脊柱骨密度(BMD)相对于基线的变化,以及血清肌酐清除率(CrCl)相 https://www.sciencedirect.com/topics/medicine-and-dentistry/creatinine对于基线的变化。
研究第48周结果显示,TAF在抗病毒能力上一点也不逊色于TDF,耐受性好,不良事件发生率低。更重要的是,与接受TDF治疗的患者相比,接受TAF治疗的患者,ALT复常率的数值更高,肾小球滤过率(eGFR)以及髋部和脊柱的骨密度损失的参数也有明显改善[20,21]。
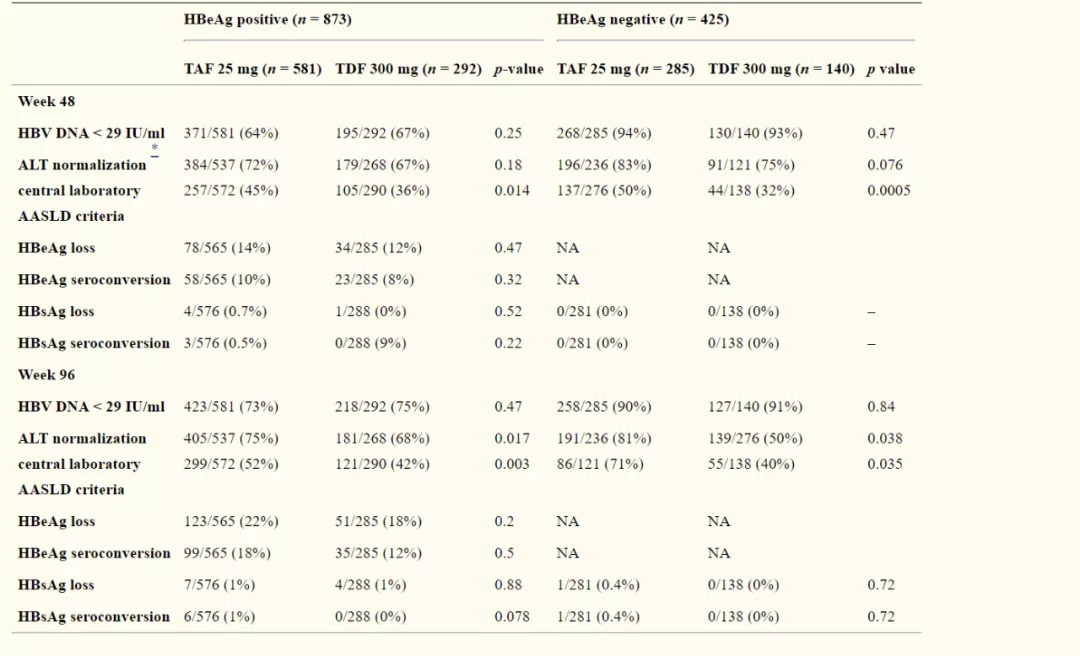 (图片来源:参考文献[22])
(图片来源:参考文献[22])
目前,两项试验的第96周[23]和第144周[24]的结果已经公布,与最初第48周试验结果也基本一致,而且第144周数据显示,两个治疗组均未检测到耐药发生[25]。
这么多的研究数据都在证明TAF的的确确是一款高效低耐药的好药。正因如此,2016年,TAF获得FDA批准,成为近几年来首个获批用于12岁以上成人的乙型肝炎治疗药物。因为其高效低耐药等特点,TAF一经上市就传来各种捷报[2]。
在美国和欧盟获批以后,2018年11月TAF又获得了中国药品监督管理局的批准,用于治疗成人和青少年(12岁以上且体重至少为35kg)的乙型肝炎[26]。最新的中国《慢性乙型肝炎防治指南(2019版)》里,TAF与ETV、TDF一起被推荐为乙型肝炎的一线抗病毒治疗药物[18]。
除108研究和110研究之外,还有很多临床研究和真实世界数据都支持了TAF在安全性以及ALT复常率上的优势。
其中在一项评估乙型肝炎病毒抑制效果III期临床试验显示,先前接受TDF治疗中位时间为4年的患者转向TAF治疗后,骨骼和肾脏标志物均得到改善[27]。
在这项研究中,研究人员先是对541例患者进行了筛查,最后选定了488名先前接受过TDF并取得病毒学抑制的受试者进行试验,将受试者随机分成转换为TAF治疗组(243人)和继续接受TDF治疗组(245人)。
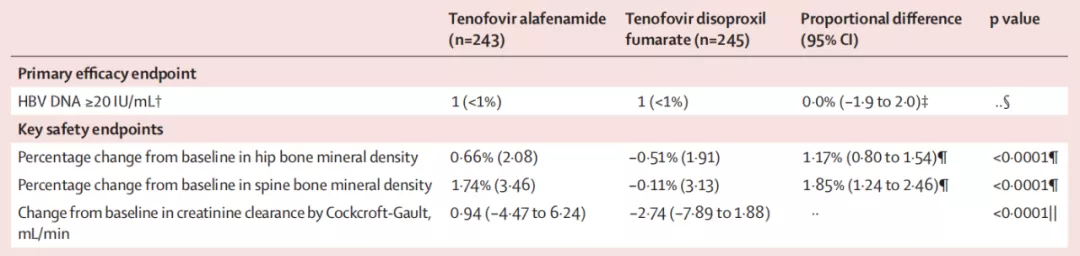 (图片来源:参考文献[27])
(图片来源:参考文献[27])
研究的主要终点是评估在病毒学抑制的慢性乙型肝炎患者中,与继续进行TDF治疗相比,从TDF转换为TAF的疗效和安全性。
研究结果显示,在患有慢性乙型肝炎的患者中,TAF不仅在疗效上不输TDF,且骨骼和肾脏安全性有明显改善,ALT的复常率也有明显的优势。
此外,研究人员还对这个研究中有TDF风险因素的患者(随机分为≥1个TDF危险因素的358人和没有TDF风险因素的130人)做了亚组分析,涉及的TDF风险因素包括,高龄、骨病、肾损害、白蛋白尿、低磷血症、肥胖以及合并症[28]。
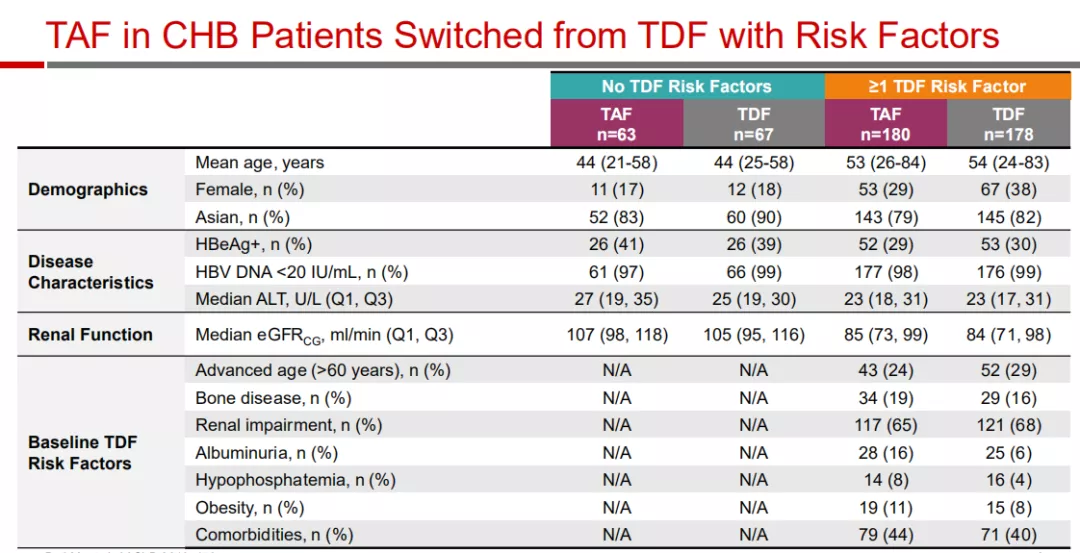 (图片来源:AASLD)
(图片来源:AASLD)
第48周的结果显示,在所有患者中,TAF维持较高的抗病毒效果。而且在至少有一个TDF危险因素的慢性乙型肝炎患者中,与继续进行TDF治疗相比,从TDF转换为TAF治疗后,他们的骨骼和肾脏参数均得到改善,ALT复常率也更高,这也与总体研究人群的结果相当。
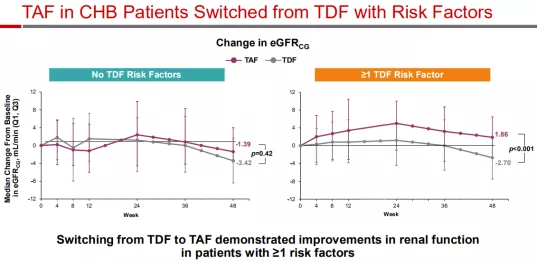 肾小球滤过滤(eGFR)指标变化情况
肾小球滤过滤(eGFR)指标变化情况
(图片来源:AASLD)
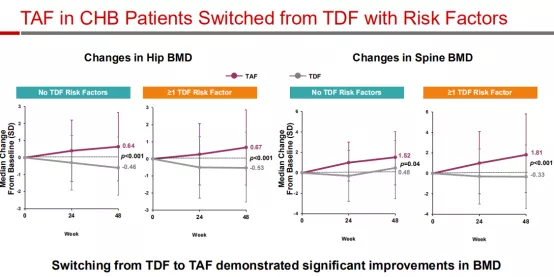 骨矿物密度(BMD)指标变化情况
骨矿物密度(BMD)指标变化情况
(图片来源:AASLD)
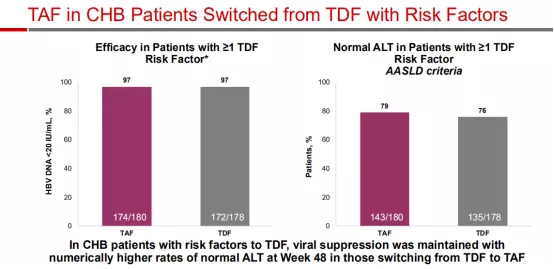 ALT指标变化情况
ALT指标变化情况
(图片来源:AASLD)
值得一提的是,在刚刚结束的2020年亚太肝病研究协会(APASL)上,又公布了该研究的新的亚组分析数据,在有TDF风险因素并取得病毒学抑制的亚裔患者中,TAF依然保持了良好疗效和安全性[29]。
 (图片来源:pixabay.com)
(图片来源:pixabay.com)
中国仍是乙型肝炎大国,时至今日,尽管有疫苗接种措施,但在乙型肝炎的治疗上面还是要面临很大的挑战。在最新一版的《慢性乙型肝炎防治指南》中显示,目前我国乙型肝炎病毒感染者仍有7000万例左右,其中发展为慢性乙型肝炎的患者约为2000万-3000万例[30]。
TAF等相关药物的出现无疑给全球尤其是中国患者带来了新的选择和希望。虽然距离实现世界卫生组织(WHO)提出到2030年消除肝炎危害的目标还有一段路要走,但是坚信为治愈而生的吉利德会再一次给患者带来惊喜。
此外,为了帮助像鲁道夫这样的罹患慢性乙型肝炎的患者有一天能够获得治愈,吉利德科学的研究团队在也积极研发新药,相信不久的将来乙型肝炎真的能从走向治愈变成实现治愈。

(来源:转自国际肝病网)
医生投稿:文章来源于医生投稿,内容仅代表作者个人观点,不代表本平台立场,转载请联系原作者。