艾滋病预防里程碑:一年两次,近乎100%保护力!长效HIV预防药获FDA批准
 健客医生官方号
健客医生官方号2025年6月18日,美国食品药品监督管理局(FDA)批准了吉利德科学公司(Gilead Sciences)开发的长效HIV暴露前预防(PrEP)药物来那帕韦(英文名:Lenacapavir;英文商品名:Yeztugo®),以降低体重≥35kg的成年及青少年群体通过性途径感染HIV的风险。
图源:吉利德官网
什么是HIV暴露前预防(PrEP)?
艾滋病一直以来都是全球公共卫生的重大挑战之一。根据世界卫生组织(WHO)的数据,截至2023年,我国HIV感染者的数量已经有131.7万。
PrEP的主要目的是为高危人群提供一种预防措施,帮助他们避免感染HIV,主要适用于还没有感染,但处于高感染风险的群体,包括:1)男男性行为者(MSM);2)注射毒品、药物成瘾者;3)性工作者;4)性活跃人群(青壮年及青少年);5)性伴侣为HIV感染者。

PrEP是一种预防性用药方案,通过阻止病毒进入人体细胞和在人体细胞中复制,从而预防高危人群感染HIV。替诺福韦酯(TDF)与恩曲他滨(FTC)(TDF/FTC)是目前PrEP最常用的方案,常规用法为每日口服一次,每次一片。
服药依从性越好,PrEP的有效性越高。但这对于不想频繁用药的患者来说,是一大挑战。
而来那帕韦是一年仅需注射两次PrEP方案。这一创新药物的获批,为艾滋病的预防带来了新的选择。
无需每天服药!一年两次,HIV预防有效率近100%
来那帕韦是一种新型的HIV-1衣壳抑制剂,它的作用机制十分独特,能够有效阻断HIV病毒生命周期中的多个关键环节,就好像给病毒设置了多重障碍,阻止病毒在人体内安家落户。
FDA的批准基于两项III期临床试验——PURPOSE 1和PURPOSE 2的数据,试验显示,来那帕韦在预防HIV感染方面表现出色,有效率接近100%。
在PURPOSE 1试验中,2134名接受来那帕韦治疗的女性中,HIV感染病例为0,预防有效率达到了100%。
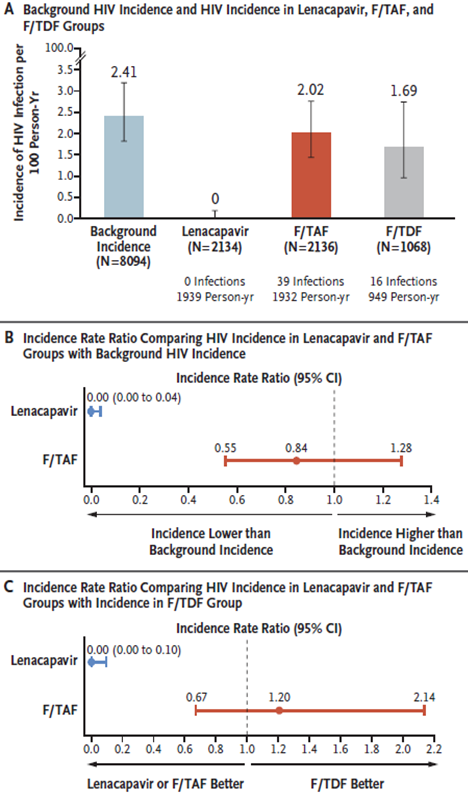
PURPOSE 1研究结果:HIV发病率汇总
在 PURPOSE 2试验中,2179名接受来那帕韦治疗的受试者中,99.9%的受试者未感染。
而且,在这两项试验中,来那帕韦均显示出良好的耐受性和安全性,未发现重大或新的安全问题。
艾滋多重耐药新选择,来那帕韦已在国内获批用于HIV治疗
来那帕韦的独特作用机制不仅在预防HIV感染方面表现出色,在治疗HIV感染方面也具有优势。
2025年1月2日,来那帕韦获国家药品监督管理局批准,用于联合其他抗反转录病毒(ARV)药物,治疗当前方案无法达到病毒学抑制的多重耐药(MDR)1型人类免疫缺陷病毒(HIV-1)感染的成人患者。

图源:国家药监局
CAPELLA研究是一项II/III期临床试验,旨在评估来那帕韦联合优化背景治疗(OBT)在多重耐药HIV-1感染者中的疗效和安全性,受试者们既往接受抗反转录病毒药物的中位数量为9种。
研究结果显示:在接受来那帕韦治疗52周后,患者病毒载量明显下降,83%的患者HIV-1 RNA降至<50 拷贝/毫升。
这些积极的结果表明,来那帕韦能够有效降低病毒载量并提高患者的免疫功能,对于多重耐药型HIV感染患者具有一定的治疗效果。
普通人预防艾滋病,如何做?
感染艾滋病病毒的途径主要有三条:血液途径传播,性途径传播,母婴途径传播。亲吻、拥抱、握手或共用个人物品、食物或水等一般日常接触不会使人们受到感染。
PrEP只是艾滋病预防一种重要手段,日常生活中还可以通过以下方式降低艾滋病毒感染风险:
远离毒品
到正规医疗机构打针、做手术
不与他人共用牙刷、剃须刀等可能刺破皮肤的生活用品
避免直接接触他人血液
固定性伴侣,性生活过程中做好防护
随着医学技术的不断进步,HIV防治领域也取得了诸多突破。来那帕韦作为一种新型的HIV PrEP药物,具有显著的预防效果和便捷的用药方式。对于那些无法坚持每日服药的高危人群而言,通过每半年注射一次来那帕韦,可以显著降低HIV感染的概率。
尽管来那帕韦在中国获批的适应症是用于治疗多重耐药HIV感染,其用于PrEP的适应症尚未在国内获批,但随着国内药物审批流程的加速推进与真实世界数据的持续积累,来那帕韦这类创新方案或将成为填补我国HIV预防“长效空白”的关键拼图,让我们一起期待!
参考文献:
1.Gilead Sciences . Yeztugo® (Lenacapavir) Is Now the First and Only FDA-Approved HIV Prevention Option Offering 6 Months of Protection. June 18, 2025. Available from: https://www.gilead.com/news/news-details/2025/yeztugo-lenacapavir-is-now-the-first-and-only-fda-approved-hiv-prevention-option-offering-6-months-of-protection
2. 国家药品监督管理局. 2025年01月02日药品批准证明文件送达信息. Available from: https://www.nmpa.gov.cn/zwfw/sdxx/sdxxyp/yppjfb/20250102154109161.html
3. Gilead Sciences . 每年两次给药的HIV长效疗法萨兰卡®在华获批. 2025年01月02日. Available from: https://mp.weixin.qq.com/s/ceVvpite5yfU_ueW4_HJyQhttps://mp.weixin.qq.com/s/ceVvpite5yfU_ueW4_HJyQ
4.杨新宇. 艾滋病暴露前预防与暴露后预防的应用与挑战[J]. 中国艾滋病性病,2019,25(4):425-428. DOI:10.13419/j.cnki.aids.2019.04.029.
5.Ogbuagu O, Segal-Maurer S, Ratanasuwan W, et al. Efficacy and safety of the novel capsid inhibitor lenacapavir to treat multidrug-resistant HIV: week 52 results of a phase 2/3 trial. Lancet HIV. 2023;10(8):e497-e505.
6.中国性病艾滋病防治协会艾滋病药物预防与阻断专委会.中国HIV暴露前预防用药专家共识(2023版)[J].中国艾滋病性病,2023,29(9):954-961.
7.中华医学会感染病学分会艾滋病学组,中国疾病预防控制中心,李太生. 中国艾滋病诊疗指南(2024版)[J]. 协和医学杂志,2024,15(6):1261-1288.
8.WHO. HIV Country Intelligence. Available from:https://cfs.hivci.org/
原创文章:方舟健客版权所有,未经许可不得转载。