医学资讯「5.9-5.22」:诺华瑞波西利乳腺癌辅助治疗获批│阿思尼布片治疗CML国内获批│BI肺纤维化新疗法登NEJM
 医周动态官方号
医周动态官方号01. 诺华CDK4/6抑制剂琥珀酸瑞波西利片早期乳腺癌辅助治疗适应症获批
5月14日,诺华中国宣布其重磅乳腺癌治疗产品琥珀酸瑞波西利片(凯丽隆®)获得国家药品监督管理局批准新增适应症,适用于与芳香化酶抑制剂联合使用,作为激素受体(HR)阳性、人类表皮生长因子受体2(HER2)阴性高复发风险的早期乳腺癌患者的辅助治疗。
乳腺癌不单是威胁全球女性健康的“第一大癌”,中国也已成为乳腺癌高发国家,数据显示,2022年中国新发乳腺癌35.72万,发病率位居女性恶性肿瘤第二位,其中有超过95%的患者确诊时为早期阶段。HR+/HER2-早期乳腺癌虽可以被治愈,但仍有高达1/3的患者即便接受了传统辅助内分泌治疗仍会复发转移,进展为不可治愈的疾病。
CDK4/6抑制剂在HR+/HER2-早期乳腺癌辅助治疗的应用,降低了早期患者复发转移风险。此次瑞波西利的获批是基于NATALEE研究,为一项III 期多中心、随机、开放标签试验,旨在评估瑞波西利(RIB) 联合非甾体芳香化酶抑制剂(NSAI)辅助治疗用于HR+/HER2-早期乳腺癌 (EBC)患者的4年结果。该试验纳入了5101名受试者,按1:1随机分配至RIB+ NSAI组和单用NSAI组。主要终点为无侵袭性疾病生存期(iDFS),次要终点为无远处转移生存期(DDFS)和总生存期(OS)。结果显示,
主要终点:
iDFS的中位随访时间为44.2个月。 RIB+NSAI联合治疗较单纯NSAI疗法显著改善iDFS(风险比(HR)=0.715;95% CI:0.609-0.840;P<0.0001)。
次要终点:
• RIB+NSAI联合治疗较单纯NSAI疗法具有DDFS获益(HR=0.715;95% CI:0.604-0.847)。
• OS仍未成熟,但趋势倾向于RIB(HR=0.827;95%CI:0.636-1.074)。
• 安全性与之前的分析结果一致。
瑞波西利辅助强化治疗相较于单纯辅助内分泌治疗,4年乳腺癌复发风险及远处转移风险均下降达28.5%,并且在包括无淋巴结转移或II期在内的各个亚组中均观察到一致的获益,进一步证明了瑞波西利辅助强化治疗在早期乳腺癌患者的持久广泛获益,未来将助力中国更多乳腺癌患者降低早期复发风险,带来治愈希望。
02. 诺华创新药物盐酸阿思尼布片在华获批,开启慢粒STAMP精准靶向治疗新时代
5月14日,诺华创新药物盐酸阿思尼布片(信倍立®)获得国家药品监督管理局批准,用于治疗新诊断的费城染色体阳性的慢性髓细胞白血病(Ph+CML)慢性期(CP)成人患者。作为全球首个且目前唯一获批基于ABL肉豆蔻酰口袋(STAMP)创新机制的靶向药物,阿思尼布可实现深度缓解率翻倍和不良事件相关停药风险减半,延缓疾病进展,为CML患者提供了全新治疗选择。
慢性髓细胞白血病(CML)也称为慢性髓性白血病、慢性粒细胞白血病,或慢粒,是一种骨髓造血干细胞克隆性增殖形成的恶性肿瘤,占成人白血病的15%,是慢性白血病最常见的类型之一。在中国,每年约有9,300例新发病例。在既往常规化疗时代,CML患者的年死亡率为15%-20%,10年生存率不到20%。
此次阿思尼布的获批是基于关键性III期ASC4FIRST试验数据,为一项III 期多中心、随机、开放标签试验,旨在对第一代和第二代酪氨酸激酶抑制剂(TKIs)治疗Ph+CML进行随机头对头比较,主要终点为达到主要分子学反应(MMR)的受试者百分比。结果显示,
在新诊断患者中,与研究者选择的第一代或第二代TKIs(伊马替尼、尼洛替尼、达沙替尼或博舒替尼)治疗方案相比,接受阿思尼布治疗的患者在第96周达到MMR(即BCR:ABL1融合基因水平≤0.1%)的人数比例较对照组显著提升(74.1%vs 52.0%,P<0.001)。
在此项研究中,阿思尼布也表现出了良好的安全性。与第一代和第二代TKIs相比,阿思尼布大于3级不良事件的发生率更低,因不良事件导致的治疗终止风险减少一半以上。
相较于TKI药物,盐酸阿思尼布片凭借其突破性机制带来了优异的疗效,安全性和耐受性。此次在中国的获批标志着这款创新药物不仅将为CML患者提供更多治疗选择,也将有望改变我国CML治疗的整体面貌,开启STAMP精准靶向治疗新时代。
03. BI肺纤维化创新疗法研究登上NEJM
Nerandomilast (BI 1015550) 是一种口服优先磷酸二酯酶4B抑制剂,具有抗纤维化和免疫调节作用。近日,《新英格兰医学杂志》(NEJM)发表了一项Nerandomilast治疗特发性肺纤维化患者的3期临床试验结果。

这是一项III期双盲试验,共纳入了1177例受试者,按1:1:1的比例将特发性肺纤维化患者随机分配至以下组:nerandomilast(每日两次,每次18mg)、nerandomilast(每日两次,每次9mg)或安慰剂组,并根据背景抗纤维化治疗(尼达尼布或吡非尼酮 vs. 无)进行分层。主要终点是第52周时用力肺活量 (FVC) 相对于基线的绝对变化量(以ml为单位)。结果显示,
• Nerandomilast 18mg组与安慰剂组之间的校正差异为68.8ml(95% CI:30.3-107.4;P<0.001):
• Nerandomilast 9mg组与安慰剂组之间的校正差异为44.9ml(95% CI:6.4-83.3;P = 0.02)。
• Nerandomilast组最常见的不良事件是腹泻,18mg组报告发生率为 41.3%,9mg组报告发生率为 31.1%,而安慰剂组报告发生率为16.0%。各试验组的严重不良事件均衡。
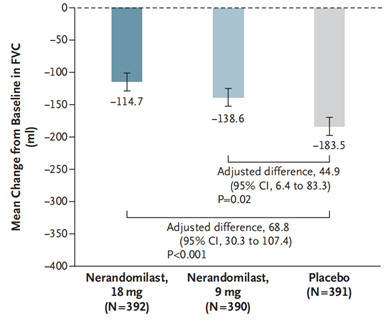
主要终点
这项研究表明,在特发性肺纤维化患者中,nerandomilast治疗52周后可显著减缓患者肺功能下降。Nerandomilast为特发性肺纤维化患者提供了潜在的治疗选择,对已接受尼达尼布或吡非尼酮治疗的患者也同样有效。
04. 默沙东新型抗菌药物注射用亚胺西瑞在华上市
2025年5月12日,默沙东宣布,其新型碳青霉烯/酶抑制剂复合制剂注射用亚胺西瑞(锐可博®)已正式在中国境内上市,首批药物已在默沙东中国杭州工厂完成包装,实现本土首发。
注射用亚胺西瑞已于2024年12月获得中国国家药品监督管理局批准,适用于治疗18岁及以上患者由敏感革兰阴性菌引起的下列感染:医院获得性细菌性肺炎和呼吸机相关性细菌性肺炎(HABP/VABP);治疗药物选择有限或无替代治疗的复杂性尿路感染(cUTI)(包括肾盂肾炎);治疗药物选择有限或无替代治疗的复杂性腹腔内感染(cIAI)。
碳青霉烯耐药肠杆菌科细菌(CRE)和碳青霉烯耐药铜绿假单胞菌(CRPA)因其高度耐药性和对患者安全的威胁,被世界卫生组织分别列为“关键优先级病原体”和“高度优先级病原体”。面对CRE和CRPA感染造成的严峻挑战,临床迫切需要更丰富的“武器库”以有效应对。注射用亚胺西瑞的上市为破解CRE和CRPA感染治疗困局带来了新选择,也将助力抗菌药物科学化管理(AMS)的持续优化——创新抗菌药物选择、减少耐药发生、改善患者预后。期待能有更多创新药物落地临床,成为应对复杂耐药菌感染的“利器”,为患者生命健康保驾护航。
参考文献:
1.诺华集团. 诺华CDK4/6抑制剂凯丽隆®早期乳腺癌辅助治疗适应症获批,助力更广泛HR+早期乳腺癌患者实现治愈. Published May 14, 2025. Accessed May 15, 2025. https://mp.weixin.qq.com/s/CeyXrLfZbSQJOld-yOBKcA
2. Fasching PA, et al. LBA13 Adjuvant ribociclib (RIB) plus nonsteroidal aromatase inhibitor (NSAI) in patients (Pts) with HR+/HER2−early breast cancer (EBC): 4-year outcomes from the NATALEE trial. Annals of Oncology. 2024 Sep 1;35:S1207.
3.诺华集团. 诺华创新药物信倍立®(盐酸阿思尼布片)在华获批,开启慢粒STAMP精准靶向治疗新时代. Published May 14, 2025. Accessed May 15, 2025. https://mp.weixin.qq.com/s/rUfmLgmBJhFucNpgf21QBQ
4. Cortes JE, Hochhaus A, Hughes TP. Asciminib Continues to Provide Superior Efficacy and Favorable Safety and Tolerability vs Tyrosine Kinase Inhibitors In Newly Diagnosed Chronic Myeloid Leukemia in ASC4FIRST: Week 96 Update. In66th ASH Annual Meeting & Exposition 2024 Dec 7.
5.Richeldi L, et al. Nerandomilast in Patients with Idiopathic Pulmonary Fibrosis. N Engl J Med. Published online May 18, 2025.
6.默沙东中国. 默沙东新型抗菌药物锐可博®(注射用亚胺西瑞)在华上市. Published May 12, 2025. Accessed May 14, 2025. https://mp.weixin.qq.com/s__biz=MjM5ODI4OTI2NA==&mid=2651977381&idx=1&sn=74dc132347dcd5b6ddbaec6a3459aadd
原创文章:方舟健客版权所有,未经许可不得转载。