全球首款!罕见病新药获FDA加速批准
 健客医生官方号
健客医生官方号罕见病治疗领域再传佳音!2026年2月23日,Immedica Pharma宣布,美国FDA加速批准罕见代谢病新药Loargys®(pegzilarginase-nbln)上市,用于联合饮食蛋白限制,治疗2岁及以上精氨酸酶1缺乏症(ARG1-D)患者的高精氨酸血症。
这款药物是全球首个被证实能降低ARG1-D患者血浆精氨酸水平的疗法,也已在欧盟、英国等地区获批,为超罕见代谢病患者带来了全新治疗希望。
ARG1-D:被“蛋白质”困住的人生
ARG1-D是一种常染色体隐性遗传的罕见代谢病,美国新生儿发病率为/1000000~1/300000,日本发病率约为1/350000,我国尚无相关流行病学调查报告。
该病属于常染色体隐性遗传病,简单来说,是由于患者体内缺乏精氨酸酶1,无法正常代谢精氨酸,导致精氨酸在血液中大量堆积,并产生神经毒性。
患者多在婴儿晚期或幼儿期确诊,主要症状包括进行性痉挛性瘫痪、认知能力的退化、身材矮小。
Loargys:精准清除体内“毒素”
ARG1-D的治疗方法主要包括饮食疗法、药物对症治疗等。此次获批的Loargys是一款重组人精氨酸酶-1,能持续降低血浆精氨酸及毒性代谢物水平。其适应症明确为2岁及以上ARG1-D患者的高精氨酸血症,但需配合饮食蛋白限制使用。
该药的获批主要基于3期PEACE临床试验,该研究证实了Loargys在降低血浆精氨酸水平和改善患者运动功能方面的双重获益:
生化指标显著改善:治疗24周后,Loargys组血浆精氨酸从 354.0μmol/L降至 86.4μmol/L(降幅高达76%),90.5%患者的指标恢复正常,而安慰剂组几乎没有变化(464.7降至426.6μmol/L)。
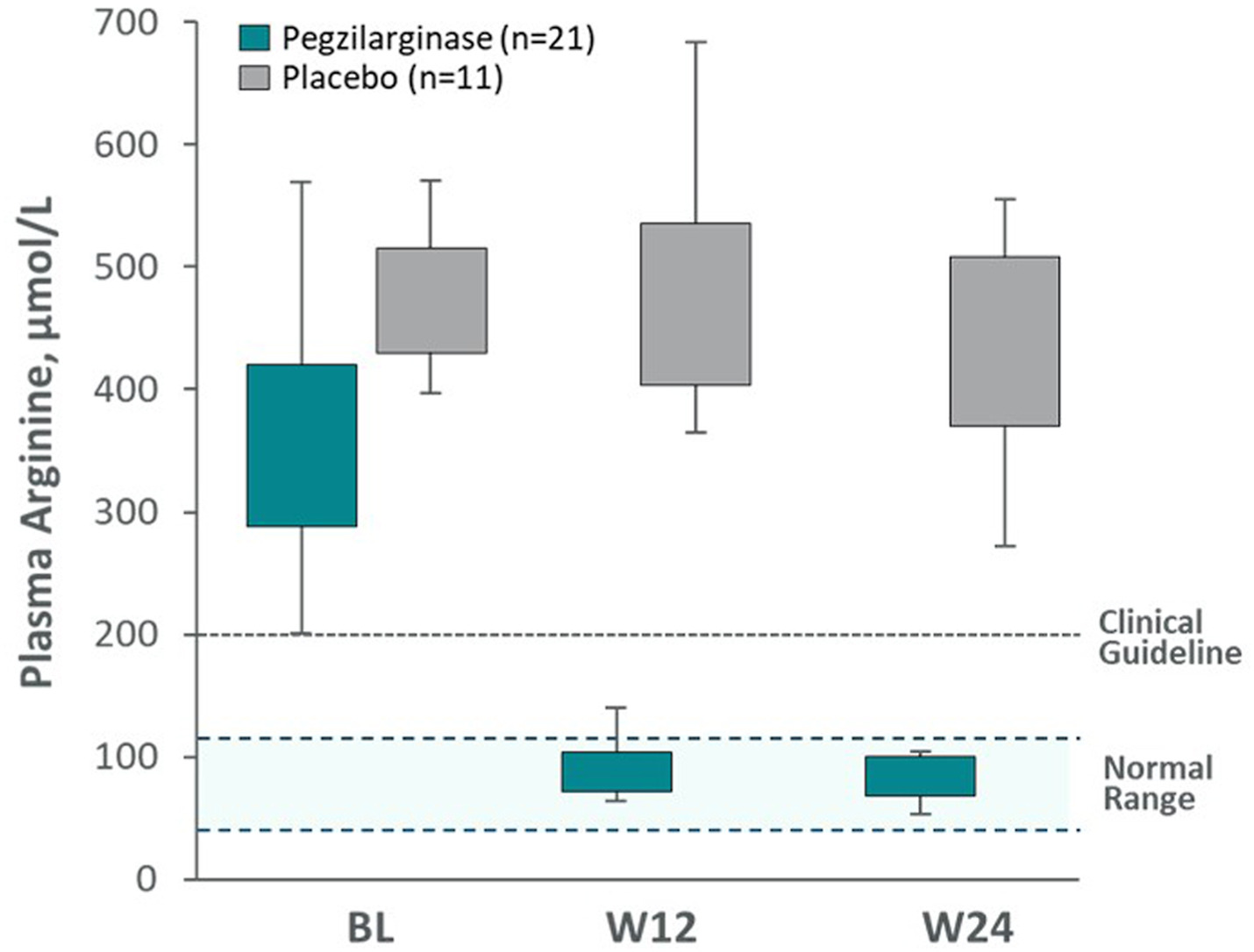
图为对血浆精氨酸水平的影响
运动功能临床获益:接受Loargys治疗的患者在粗大运动功能量表(GMFM-D/E)和2分钟步行测试(2MWT)中表现出临床意义上的改善。这意味着患者可能走路更稳、行走距离更长,生活质量得到提升。
安全性上,Loargys整体耐受性良好,13%患者出现轻中度超敏反应,常见不良反应为呕吐、发热、输注相关反应等。
Loargys的获批,不仅填补了ARG1-D病因治疗的空白,让这种原本进展性的致残疾病有望成为可早期干预的可控慢性病,也为其他罕见尿素循环障碍、氨基酸代谢病的药物研发提供了重要参考。
对于ARG1-D患者及其家庭而言,Loargys的出现不仅是药物的突破,更是扭转命运的曙光。
参考文献:
1.https://loargys.eu/wp-content/uploads/2025/06/Loargys_API.pdf
2.U.S. FDA has granted accelerated approval of Loargys® (pegzilarginase-nbln) for the treatment of hyperargininemia in patients 2 years and older with Arginase 1 Deficiency (ARG1-D)
3.Russo RS, Gasperini S, Bubb G, et al. Efficacy and safety of pegzilarginase in arginase 1 deficiency (PEACE): a phase 3, randomized, double-blind, placebo-controlled, multi-centre trial. EClinicalMedicine. 2024;68:102405. Published 2024 Jan 12.
4.国家卫生健康委. 罕见病诊疗指南(2019年版): 精氨酸酶缺乏症:32-35.
原创文章:方舟健客版权所有,未经许可不得转载。