欧盟重磅批准!吉利德半年一针HIV预防方案落地欧洲,推动全球抗艾战略再升级
 医学热点官方号
医学热点官方号欧盟批准来那帕韦用于HIV暴露前预防[1]
2025年8月26日,吉利德科学(Gilead Sciences)宣布,其长效HIV-1衣壳抑制剂来那帕韦(lenacapavir,商品名:Yeztugo®)已获得欧盟委员会(EC)批准,用于高风险成人及青少年(体重≥35kg)的HIV暴露前预防(PrEP)。该疗法每年仅需注射两次,是欧盟境内首个获批的半年一次长效PrEP方案。
这一里程碑式批准不仅覆盖欧盟27个成员国,还包括欧洲经济区的挪威、冰岛和列支敦士登,标志着欧洲在HIV防控领域迎来全新时代。
 图源:吉利德官网[1]
图源:吉利德官网[1]
EC的快速决策得益于欧洲药品管理局(EMA)人用药品委员会(CHMP)此前的积极评价,认为来那帕韦在HIV防控中具有重大的公共卫生价值。与既往每日口服PrEP方案相比,半年一次的长效注射被视为提升依从性、降低新发感染率的重要突破。
已在美国与中国先行获批[2-3]
在欧盟获批之前,来那帕韦已于2025年6月18日获得美国食品药品监督管理局(FDA)的批准,成为美国首个半年一次的HIV PrEP方案。
同年7月,世界卫生组织(WHO)也在最新指南中,将半年一次的来那帕韦推荐为额外的PrEP选择。
在中国,国家药品监督管理局(NMPA)已于2025年1月批准来那帕韦注射液及片剂上市,不过其获批适应症为联合其他抗逆转录病毒药物治疗多重耐药HIV-1感染的成人患者,主要聚焦于治疗领域。
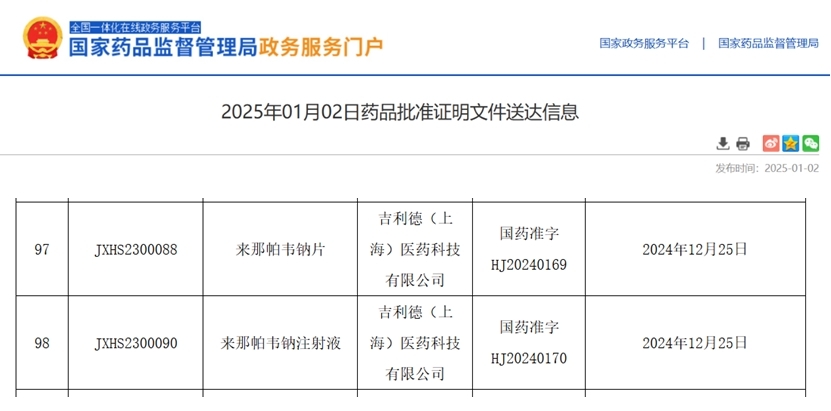 图源:中国国家药监局(NMPA)官网[3]
图源:中国国家药监局(NMPA)官网[3]
这意味着,来那帕韦在治疗与预防两条路径上均已获得国际主流监管机构的认可,形成了全球HIV防控领域的一次重大突破。
PURPOSE研究奠定循证基础:预防有效率近100%[1,4]
欧盟的批准主要基于PURPOSE 1与PURPOSE 2两项关键性III期临床试验的数据,这些研究结果均发表于《新英格兰医学杂志》(NEJM),并被《Science》杂志评为“2024年度科学突破”。
· PURPOSE 1(NCT04994509):在非洲地区2134名顺性别女性中,半年一次皮下注射来那帕韦组无一例HIV感染,表现出100%预防有效率,并显著优于每日口服Truvada®(恩曲他滨/富马酸替诺福韦)。
· PURPOSE 2(NCT04925752):在2179名顺性别男性及性别多元人群中,仅发现2例HIV感染,整体预防有效率达99.9%,同样优于每日口服PrEP方案。
两项研究还显示,来那帕韦在各类高风险人群中均表现出优异的耐受性,未发现新的安全性问题。
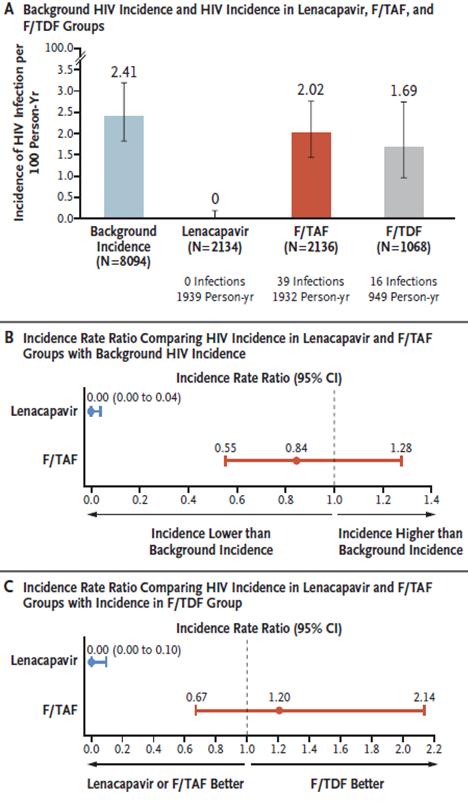 PURPOSE 1研究结果:HIV发病率汇总[4]
PURPOSE 1研究结果:HIV发病率汇总[4]
药物机制与优势[1]
来那帕韦是一种“first-in-class”长效艾滋病毒衣壳抑制剂,与现有的抗逆转录病毒药物不同,来那帕韦通过作用于病毒生命周期的多个阶段——包括病毒衣壳的组装与拆卸、病毒核进入及释放等,从而实现对HIV复制的多点抑制。这一独特作用机制不仅保证了强效的抑制能力,同时在体外研究中显示对既往药物耐药株仍具有活性。
根据欧洲疾控中心数据,欧盟及欧洲经济区每年约有2.5万例新增HIV感染病例,现有PrEP手段尚未覆盖所有高风险人群。传统每日口服药物虽然有效率高,但受制于依从性不足、社会污名、服药隐私压力等问题,实际使用率远低于理想水平。
更重要的是,来那帕韦这一长效注射剂型(每6个月一次)突破了口服PrEP需每日服药的依从性瓶颈,大大提升了预防策略的可行性与人群接受度,能够显著缓解上述痛点。
结 语
来那帕韦在欧盟的获批,标志着HIV预防领域进入了长效化与低频给药的新阶段。继美国和中国之后,欧盟的加入不仅是对其临床价值的再次肯定,更意味着全球范围内HIV防控格局的重大改变。未来,随着更多国家的批准与可及策略的推进,半年一次的HIV防控方案有望成为全球抗击HIV流行的重要支柱。
参考:
1. Gilead Sciences .European Commission Authorizes Twice-Yearly Yeytuo® (Lenacapavir) for HIV Prevention. August 26, 2025. Available from: https://www.gilead.com/news/news-details/2025/european-commission-authorizes-twice-yearly-yeytuo-lenacapavir-for-hiv-prevention
2. Gilead Sciences . Yeztugo® (Lenacapavir) Is Now the First and Only FDA-Approved HIV Prevention Option Offering 6 Months of Protection. June 18, 2025. Available from: https://www.gilead.com/news/news-details/2025/yeztugo-lenacapavir-is-now-the-first-and-only-fda-approved-hiv-prevention-option-offering-6-months-of-protection
3. 国家药品监督管理局. 2025年01月02日药品批准证明文件送达信息. Available from: https://www.nmpa.gov.cn/zwfw/sdxx/sdxxyp/yppjfb/20250102154109161.html
4. Bekker LG, Das M, Abdool Karim Q, et al. Twice-Yearly Lenacapavir or Daily F/TAF for HIV Prevention in Cisgender Women. N Engl J Med. 2024 Jul 24. doi: 10.1056/NEJMoa2407001.
原创文章:方舟健客版权所有,未经许可不得转载。