2025 ACC科学声明:告别「唯LDL论」,炎症指标如何纳入心血管风险评估与治疗决策?
 医学热点官方号
医学热点官方号近年来,多层证据把“炎症-免疫”明确地嵌入了动脉粥样硬化与心力衰竭的病理图谱之中,如NLRP3炎症小体介导的IL-1β/IL-6级联被证实是斑块发生、演进与临床事件触发的关键环节;巨噬细胞、T细胞等多类免疫细胞在内皮功能障碍、脂质沉积、纤维帽重塑与斑块破裂的不同时相承担异质化角色,炎症驱动的免疫反应则加速斑块不稳定并提升急性事件风险[1]。这一机制框架与临床观察互相印证,即便传统危险因素得到优化,残余炎症仍可独立预示再发事件。
在临床转化层面,抗炎治疗已实质性进入二级预防。CANTOS与COLCOT等大型随机对照试验分别验证了IL-1β抑制剂与小剂量秋水仙碱对主要不良心血管事件(MACE)的显著降低效应,其中秋水仙碱已获美国FDA用于动脉粥样硬化性心血管疾病人群的二级预防批准,成为降脂之外的可操作“第二把钥匙”[2]。与此同时,IL-6受体拮抗剂以及NLRP3特异性抑制剂(如 MCC950)等新型抗炎策略正在推进临床试验,初步信号指向良好前景[3]。可以预见,抗炎不再是“锦上添花”的探索,而是与降脂、控压、控糖并列的治疗维度。此前,2002年的科学声明在证据不足的前提下,提示在整体人群中并不主张普遍炎症标志物筛查[4]。
2025年9月,美国心脏病学会(ACC)正式发布《炎症与心血管疾病:2025 ACC科学声明》(Inflammation and Cardiovascular Disease: 2025 ACC Scientific Statement)[5]。这份科学声明以“炎症”为核心线索的系统重构,把残余炎症风险拉回心血管临床一线,给出了覆盖筛查—评估—影像—一/二级预防—心衰—复发性心包炎—生活方式的整合建议,并以高质量随机证据为锚,明确哪些该立刻做、哪些仍处研究前沿。本文尝试以医生关切为中心,从“能做什么、为谁做、何时做、做到什么程度”四个问题出发,串联证据与实践路径。
评价与风险分层:以hsCRP为轴的测-评-管闭环[5]
1) 生物标志物
声明明确指出,即便在血脂控制理想的患者中,若炎症指标,尤其是高敏C反应蛋白(hsCRP) 持续升高,其心血管事件风险依然居高不下。这种现象被称为残余炎症风险(Residual inflammatory risk),已成为当前心血管二级预防中最被低估的盲区。
hsCRP的风险信息量可与LDL-C、血压并列,其长期稳定性与变异度与LDL-C、血压相当;与此同时,对hsCRP的临床解释阈值通常为<1、1–3、>3 mg/L 表示低、中、高相对风险,>10 mg/L宜排除急性感染/应激并复测。声明建议:
• 其他炎症生物标志物(如 SAA、IL-6、纤维蛋白原、白细胞计数、中性粒/淋巴细胞比值、EPA/AA比值)也能预测风险;然而常规评估这些指标对hsCRP的增益有限,且仅hsCRP被监管机构认可并在主要心血管结局试验中持续使用。
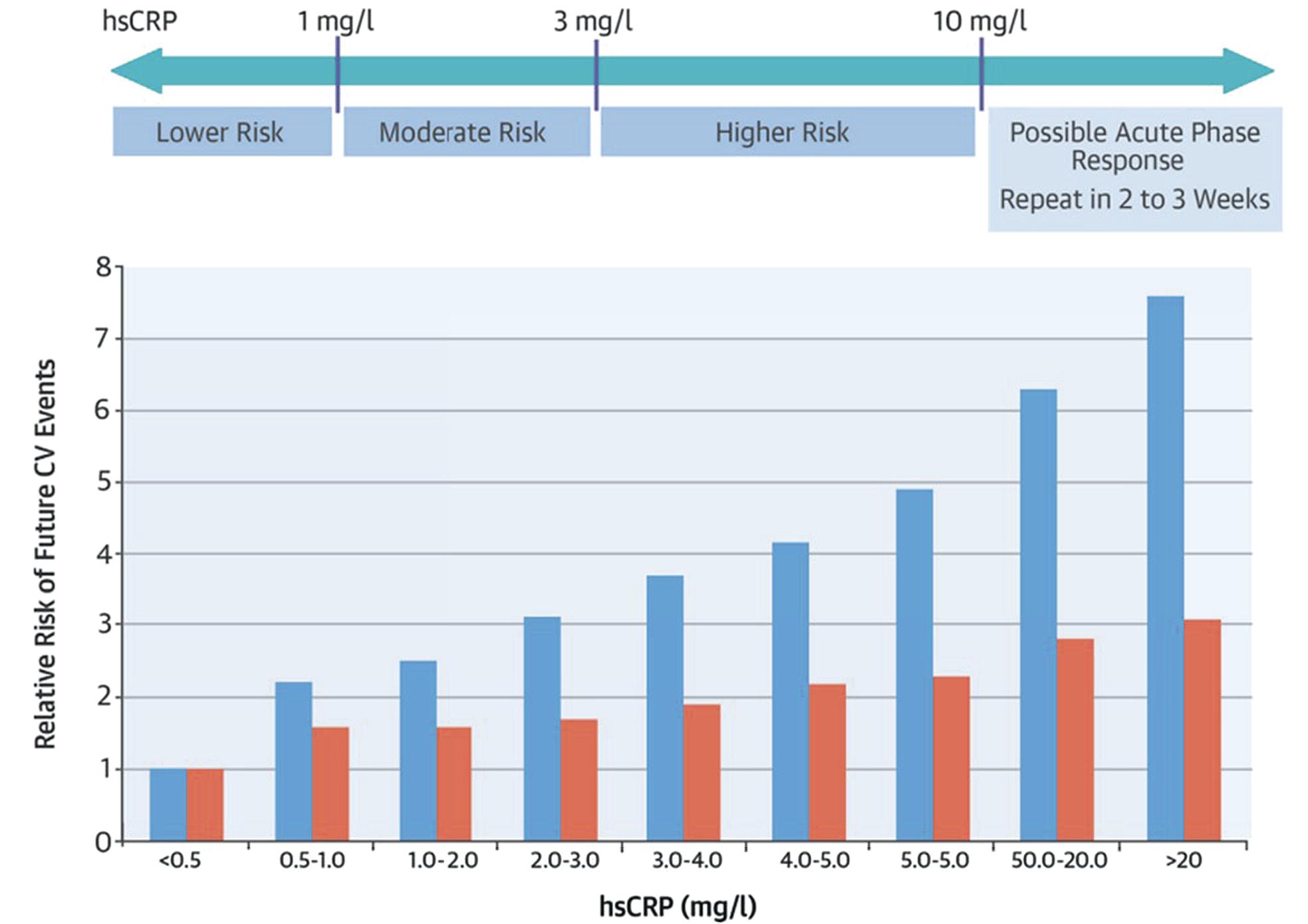 hsCRP与心血管风险的线性关系[5]
hsCRP与心血管风险的线性关系[5]
2)影像生物标志物
非侵入性影像(CT、MRI、超声、FDG-PET 等)为识别斑块/周血管炎症提供可能,CT-FAI 在队列中可独立预测冠脉事件,但当前仍主要用于研究;并未建议常规临床使用。
• 声明中推荐:用于检测血管炎症的影像生物标志物很有前景,但不应在常规临床环境使用。
 用于非侵入性检测血管炎症的影像学技术及优缺点概览[5]
用于非侵入性检测血管炎症的影像学技术及优缺点概览[5]
hsCRP与原发预防:阈值、基线风险与药物信号[5]
流行病学与随机对照试验证实:在LDL-C正常的人群内,hsCRP升高提示更高首次事件风险;JUPITER 研究在LDL-C<130 mg/dL且hsCRP≥2 mg/L的个体中,20 mg瑞舒伐他汀显著降低复合终点,且对“无传统可修饰危险因素但炎症升高”的亚群同样有效。因此,声明建议:
• 当患者无急性感染或疾病时,一次 hsCRP 测量(>3 mg/L)可用于识别炎症风险升高的原发预防个体;
• 对于炎症负荷上升的个体,早期启动生活方式干预被推荐以降低炎症风险;
• 在原发预防中,若hsCRP持续升高,应考虑启动或强化他汀治疗,无论LDL-C水平如何。
• 另外,声明提及药物因素可影响hsCRP水平,如苯哌地酸可使hsCRP降低约20%–30%,幅度与其LDL-C下降相仿,但在无ASCVD的原发预防人群中是否转化为结局获益仍未知,需要更大规模试验证实。
hsCRP与继发预防:残余炎症风险与抗炎试验的“成与败” [5]
在他汀时代的大型试验/注册研究中,hsCRP>2 mg/L的患者即便LDL-C <70 mg/dL,复发事件风险仍然居高。在84,399例瑞典动脉粥样硬化患者注册研究中,60%的受试者hsCRP >2 mg/L,提示现实世界的抗炎未满足。
另外,CANTOS研究显示:靶向 IL-1→IL-6→CRP通路的Canakinumab在稳定型、他汀治疗的患者中将复发血管事件减少15%–17%,但因适应证与可及性,并未用于心血管常规治疗。
值得一提的是,秋水仙碱低剂量(0.5 mg/d)在随机对照临床试验中,对慢性稳定动脉粥样硬化患者复合事件降低达25%,并已获FDA批准用于既往ASCVD或伴多种高危因素成人的复发事件风险降低;但在急性ST段抬高型心肌梗死(STEMI)早期使用未显示获益,提示抗炎干预的时机依赖性。
因此,声明建议:
• 在已确诊CVD人群(不论是否使用他汀)中,hsCRP预测复发事件的能力至少与LDL-C相当,体现出当代实践中残余炎症风险的重要性;
• 在已用他汀的个体中,若hsCRP仍>2 mg/L,应考虑加大到高强度剂量,无论LDL-C水平如何;
• 低剂量秋水仙碱可减少慢性稳定动脉粥样硬化患者的心血管事件,且是首个获FDA批准用于此目的的抗炎药物;
• 低剂量秋水仙碱用于脂质降低的辅助,而在急性缺血时起始并未证实有效;肝肾功能明显异常者应避免使用。
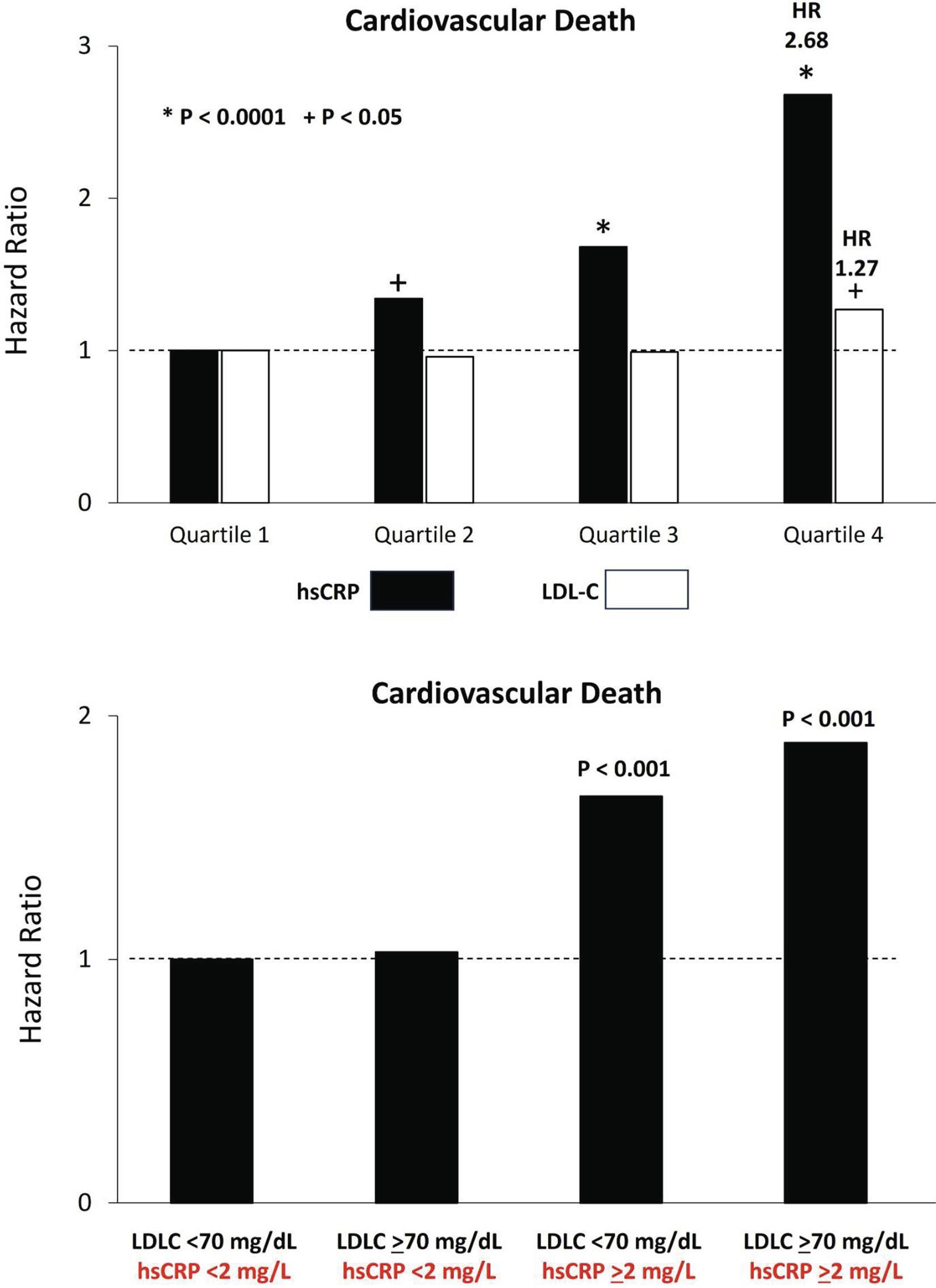
残余炎症风险与残余胆固醇风险:他汀治疗后心血管死亡风险的双轨预测[5]
(上图显示,在他汀治疗后,hsCRP升高(黑色)较LDL胆固醇升高(白色)更强地预测心血管死亡风险;下图显示,即使LDL胆固醇已控制较低,若hsCRP持续升高,心血管死亡风险依然显著增加;反之,hsCRP较低者即便LDL胆固醇略高,其风险仍较低)
生活方式干预是最基础的“抗炎处方” [5]
声明特别强调,生活方式干预是控制炎症的基石。以下是声明推荐的抗炎生活方式:
• 注重抗炎饮食模式,如地中海饮食或DASH饮食。
强调摄入水果、蔬菜、全谷物、豆类、坚果和橄榄油。
增加膳食中ω-3脂肪酸的摄入;推荐每周2-3餐鱼类(优选富含EPA+DHA的脂肪鱼)。
减少红肉和加工肉类、精制碳水化合物和含糖饮料的摄入。
• 每周进行≥150分钟的中等强度或75分钟的高强度运动。
• 戒烟以减轻慢性低度炎症。
• 保持健康体重以减轻全身性炎症。
 炎症在动脉粥样硬化发生发展中的核心桥梁:危险因素通过炎症信号通路驱动动脉病变[5]
炎症在动脉粥样硬化发生发展中的核心桥梁:危险因素通过炎症信号通路驱动动脉病变[5]
(上方展示了多种动脉粥样硬化危险因素,它们通过诱导促炎细胞因子(IL-1、TNF-α)促进斑块形成(左),并经“信使”IL-6触发肝脏急性期反应(右);下方示意急性期反应产物:包括参与动脉粥样血栓形成的因子(如纤维蛋白原、PAI-1)及可在外周血检测的标志物(如CRP、SAA);中部为减轻炎症与血栓形成的保护性因素,如饮食与运动)
心衰与复发性心包炎[5]
慢性心衰患者普遍存在免疫系统激活和炎症因子升高。CANTOS事后分析显示,Canakinumab可降低心衰住院风险。另外,在以NSAIDs+秋水仙碱为基础的标准治疗之外,对hsCRP>10 mg/L的复发性心包炎病例,随机试验证实IL-1阻断显著降低复发。
因此,声明建议:
• hsCRP、IL-6等炎症/免疫标志物可作为慢性心衰的风险预测指标;EPA+DHA可被考虑用于NYHA II–IV心衰患者的管理,不受病因或LVEF限制。
• 他汀可被考虑用于缺血性心衰且年龄>60岁的患者管理。
• 在无结核的前提下,对多次复发且对秋水仙碱与激素抵抗、且hsCRP>10 mg/L的患者,可考虑IL-1阻断。
如果说降脂时代的指标是LDL越低越好,那么抑炎时代的临床口号或许是:LDL与CRP需双轨并行。
参考文献:
1. Caldarelli M, Franza L, et al. Inflammasomes in Cardiovascular Diseases: Current Knowledge and Future Perspectives. Int J Mol Sci. 2025;26(12):5439.
2. Libby P. Targeting Inflammatory Pathways in Cardiovascular Disease: The Inflammasome, Interleukin-1, Interleukin-6 and Beyond. Cells. 2021;10(4):951.
3. Potere N, Bonaventura A, Abbate A. Novel Therapeutics and Upcoming Clinical Trials Targeting Inflammation in Cardiovascular Diseases. Arterioscler Thromb Vasc Biol. 2024;44(12):2371-2395.
4. Pearson TA, Mensah GA, et al. Markers of inflammation and cardiovascular disease: application to clinical and public health practice: a statement for healthcare professionals from the Centers for Disease Control and Prevention and the American Heart Association. Circulation. 2003;107:499–511.
5. Mensah GA, Arnold N, Prabhu SD, Ridker PM, Welty FK. Inflammation and Cardiovascular Disease: 2025 ACC Scientific Statement: A Report of the American College of Cardiology. J Am Coll Cardiol. Published online September 29, 2025.
原创文章:方舟健客版权所有,未经许可不得转载。